Węgiel (łac. carboneum) jest pierwiastkiem chemicznym o symbolu C o liczbie atomowej 6. Należy do grupy 14 układu okresowego, jest niemetalem. Posiada cztery elektrony walencyjne. Istnieją trzy naturalnie występujące izotopy węgla, 12C oraz 13C są stabilne, natomiast izotop 14C jest promieniotwórczy o czasie połowicznego rozpadu równym około 5700 lat. Węgiel jest jednym z niewielu pierwiastków znanych w starożytności. Jako pierwszy polską nazwę - węgiel - zaproponował Filip Walter.
Znanych jest kilka odmian alotropowych węgla, z czego najbardziej znane to grafit oraz diament. Właściwości fizyczne węgla zależą od odmiany w jakiej występuje. Na przykład diament jest przezroczysty, natomiast grafit jest nieprzezroczysty i czarny. Diament jest jednym z najtwardszych materiałów na ziemi, podczas gdy grafitem można narysować kreskę na papierze. Diament ma bardzo niskie przewodnictwo właściwe, a grafit jest dobrym przewodnikiem elektrycznym. Diament posiada najwyższą przewodność cieplną z wszystkich znanych materiałów w warunkach normalnych. Wszystkie odmiany alotropowe węgla są w warunkach normalnych ciałami stałymi. Innymi odmianami alotropowymi węgla są: fuleren oraz formy poliynowe. Niektórzy uważają też, że jego odmianami alotropowymi są: nanocebulka, nanorurka, nanopianka, karbin choć są to raczej nazwy struktur supramolekularnych niż odmiany alotropowe w pełnym tego słowa znaczeniu.
Wszystkie formy występowania węgla są wysoce stabilne, wymagają wysokiej temperatury żeby przereagować nawet z tlenem. Najczęściej występuje ma +4 stopniu utlenienia, oraz na +2 w tlenku węgla oraz związkach kompleksowych. Największe ilości nieorganicznego węgla występuje w postaci skał wapiennych, dolomitów oraz dwutlenku węgla, natomiast znaczne ilości węgla organicznego znajdują się w węglach kopalnych, torfie, olejach oraz w klatratach metanu. Węgiel tworzy więcej związków niż wszystkie inne pierwiastki chemiczne, których ilość dochodzi do dziesięciu milionów otrzymanych związków, co jest małą częścią teoretycznych związków jakie można z niego otrzymać.
Węgiel znajduje się na czwartym miejscu najczęściej występujących pierwiastków we Wszechświecie, po wodorze, helu i tlenie. Jest obecny we wszystkich organizmach żywych. W ludzkim ciele jest po tlenie najliczniejszym pierwiastkiem ze względu na masę (ok. 18,5%). Ta ilość w połączeniu z różnorodnością związków organicznych stawia węgiel jako chemiczną podstawę życia.
Charakterystyka

Diament i grafit są dwoma odmianami alotropowymi węgla: różnymi formami tego samego pierwiastka różniące się strukturami.
Różne odmiany alotropowe węgla wykazują bardzo różne właściwości, np. diament jest najtwardsza naturalnie występującą substancją, grafit jest jedną z substancji o najmniejszej twardości. Ponadto węgiel ma powinowactwo do tworzenia wiązań chemicznych z innymi małymi atomami, włączając w to inne atomy węgla oraz tworzenia wielu wiązań kowalencyjnych z tymi atomami w wyniki czego związki zawierające węgiel w swojej strukturze stanowią znaczną cześć wszystkich znanych związków, liczba ich dochodzi do dziecięciu milionów. Węgiel posiada także najwyższe temperatury topnienia oraz sublimacji z wszystkich pierwiastków. Przy ciśnieniu atmosferycznym nie występuje w ogóle topnienie węgla, a jego punkt potrójny występuje przy 10 MPa (100 bar) więc sublimuje on powyżej 4000K. Węgiel sublimuje do łuku węglowego w temperaturze ok. 5800K. więc niezależnie od odmian alotropowych węgiel pozostaje w ciałem stałym w wyższych temperaturach niż metale o najwyższych temperaturach topnienia (wolfram i ren). Jednakże termodynamicznie węgiel bardzo łatwo się utlenia, znacznie lepiej niż żelazo czy miedź które są słabymi reduktorami a temperaturze pokojowej.
Związki zawierające węgiel są podstawą życia na Ziemi a cykl węglowo-azotowo-tlenowy dostarcza część energii wytwarzanej przez Słońce i inne gwiazdy. Pomimo różnorodności związków węgla większość tych form jest stosunkowo słabo reaktywna w warunkach normalnych. Nie reaguje z kwasem siarkowym (VI), kwasem solnym, chlorem ani zasadami. W podwyższonej temperaturze węgiel reaguje z tlenem tworząc tlenki węgla, oraz redukuje wiele tlenków metali, takich jak tlenek żelaza, do metalu. Ta egzotermiczna reakcja jest używana w przemyśle żelazowym i stalowym do kontroli zawartości węgla w stali:
- Fe3O4+ 4C(s) → 3Fe(s) + 4CO(g)
Z siarką tworzy dwusiarczek węgla, a z parą wodna tlenek węgla i wodór:
- C(s) + H2O(g) → CO(g) + H2(g)
Węgiel reaguje z niektórymi metalami tworząc węgliki, takie jak węglik żelaza (cementyt), Węglik wolframu który dzięki swojej twardości jest używany w różnego rodzaju narzędziach tnących.
Odmiany alotropowe węgla
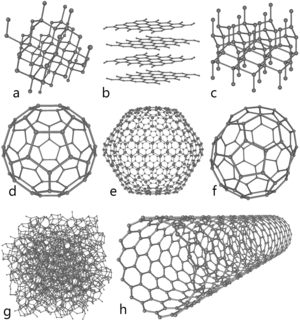
Odmiany alotropowe węgla:
a) diament, b) grafit, c) lonsdaleit
d) fuleren C60 e) fuleren C540 f) fuleren C70
g) węgiel amorficzny, h) nanorurka
Węgiel posiada następujące odmiany alotropowe:
- grafit
- diament
- fuleren
- formy poliynowe
Niektórzy uważają też, że jego odmianami alotropowymi są:
- nanocebulka
- nanorurka
- nanopianka
- karbin
choć są to raczej nazwy struktur supramolekularnych niż odmiany alotropowe w pełnym tego słowa znaczeniu.
Występowanie
Naturalne złoża węgla kamiennego i węgla brunatnego to mieszanina węgla w postaci grafitu, sadzy i różnego rodzaju zanieczyszczeń. Zawartość węgla w skorupie ziemskiej wynosi 0,018%.
-W postaci pierwiastka chemicznego:
- jako grafit
- diament
- fullereny
-W postaci związków chemicznych:
- nieorganicznych (dwutlenek węgla [CO2], tlenek węgla [II]), sole kwasu węglowego-węglany CaCO3
- organicznych - białka, tłuszcze i cukry, węglowodory, alkohole, estry itp.
-W mieszaninach jakimi są paliwa kopalne:
- gaz ziemny
- ropa naftowa
- węgiel kamienny
- torf i antracyt
Obieg węgla
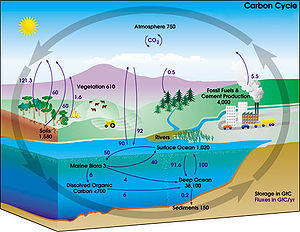
Diagram przedstawiający obieg węgla w przyrodzie.
W ziemskich warunkach, zmiana jednego związku w drugi jest rzadka. jednak ilość węgla na ziemi jest stała. Dlatego musi istnieć proces powodujący utrzymanie równej ilości węgla w różnych częściach ziemi. Ścieżki jakimi "wędruje" węgiel tworzą obieg węgla w przyrodzie. Np. rośliny pochłaniają dwutlenek węgla z powietrza i używają go do produkcji biomasy w procesie fotosyntezy lub cyklu Calvina. Część biomasy produkowanej przed rośliny zostaje zjedzona przed zwierzęta, podczas gdy część węgla jest wydychana w postaci dwutlenku węgla.
Związki węgla
Liczba znanych związków węgla jest ponad 10 razy większa niż liczba wszystkich znanych związków innych pierwiastków. Wynika to głównie z jego znaczenia biologicznego, ponieważ związki czterowartościowe węgla łączą się ze sobą tworząc np.: węglowodory. Oprócz organicznych związków węgla duże znaczenie mają też dwutlenek węgla, tlenek węgla, kwas węglowy, węglany oraz węgliki. Powszechnie stosowany jest w stopach z żelazem (stal i żeliwo).
Znaczenie biologiczne węgla
Węgiel stanowi podstawę życia na Ziemi, ponieważ tworzy wszystkie związki organiczne.
Zastosowanie węgla
Węgiel jest jednym z paliw kopalnych i ważnym źródłem nieodnawialnej energii. Uważa się, że spalanie węgla, a także innych kopalnych paliw przyczynia się do powstawania efektu cieplarnianego.
Izotop 14C używany jest do datowania. W czasie życia w organizmie żywym przyswajane są związki z węglem 14C, i odkładane wewnątrz tkanek. Po śmierci węgiel rozpada się. Podczas określania wieku organizmu mierzy się proporcję azotu do węgla.
Grafit jest stosowany w poligrafii do produkcji ołówków oraz jako jedna z elektrod w spawalnictwie. Diament jest kamieniem szlachetnym stosowanym w jubilerstwie oraz ze względu na swoją wysoką twardość w urządzeniach pomiarowych, narzędziach do skrawania, zwłaszcza szlifowania i wiercenia. Węgiel bezpostaciowy jest używany w medycynie oraz jako węgiel aktywny do procesów filtracji i oczyszczania.

